Anugerah Penyelidikan Perubatan Asas Lasker tahun ini telah dianugerahkan kepada Demis Hassabis dan John Jumper atas sumbangan mereka kepada penciptaan sistem kecerdasan buatan AlphaFold yang meramalkan struktur tiga dimensi protein berdasarkan urutan urutan pertama asid amino.
Keputusan mereka menyelesaikan masalah yang telah lama menyusahkan komuniti saintifik dan membuka pintu untuk mempercepatkan penyelidikan merentasi bidang bioperubatan. Protein memainkan peranan penting dalam perkembangan penyakit: dalam penyakit Alzheimer, mereka berlipat dan bergumpal bersama; Dalam kanser, fungsi pengawalseliaan mereka hilang; Dalam gangguan metabolik bawaan, ia tidak berfungsi; Dalam fibrosis kistik, mereka pergi ke ruang yang salah dalam sel. Ini hanyalah beberapa daripada banyak mekanisme yang menyebabkan penyakit. Model struktur protein terperinci boleh menyediakan konfigurasi atom, memacu reka bentuk atau pemilihan molekul pertalian tinggi dan mempercepatkan penemuan ubat.
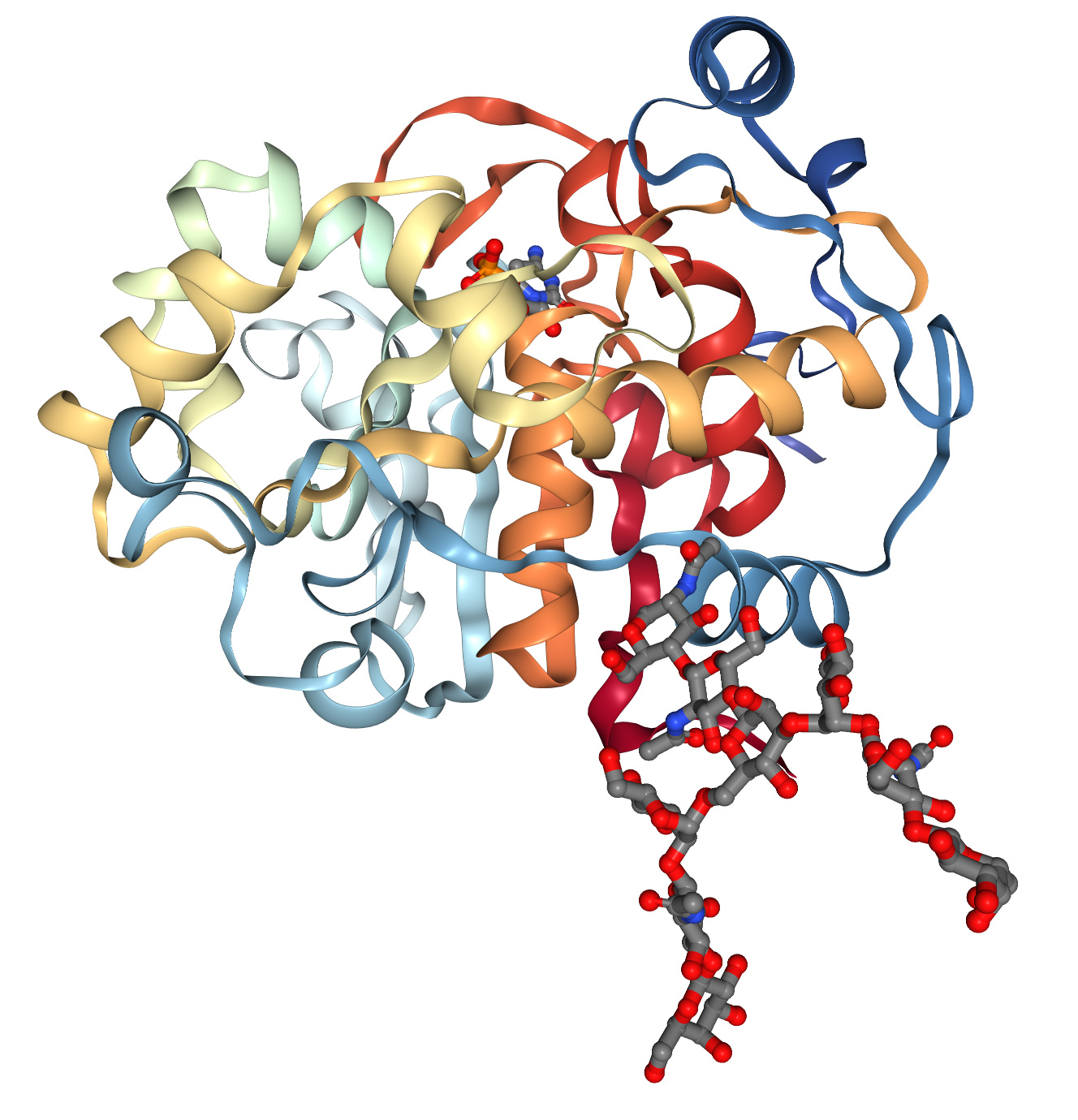
Struktur protein biasanya ditentukan oleh kristalografi sinar-X, resonans magnetik nuklear dan mikroskopi cryo-elektron. Kaedah ini mahal dan memakan masa. Ini menghasilkan pangkalan data struktur protein 3D sedia ada dengan hanya kira-kira 200,000 data struktur, manakala teknologi penjujukan DNA telah menghasilkan lebih daripada 8 juta jujukan protein. Pada tahun 1960-an, Anfinsen et al. mendapati bahawa urutan 1D asid amino boleh secara spontan dan berulang kali dilipat menjadi bentuk tiga dimensi yang berfungsi (Rajah 1A), dan "chaperones" molekul boleh mempercepat dan memudahkan proses ini. Pemerhatian ini membawa kepada cabaran 60 tahun dalam biologi molekul: meramalkan struktur 3D protein daripada urutan 1D asid amino. Dengan kejayaan Projek Genom Manusia, keupayaan kami untuk mendapatkan jujukan asid amino 1D telah bertambah baik, dan cabaran ini menjadi lebih mendesak.
Meramalkan struktur protein adalah sukar untuk beberapa sebab. Pertama, semua kemungkinan kedudukan tiga dimensi bagi setiap atom dalam setiap asid amino memerlukan banyak penerokaan. Kedua, protein menggunakan maksimum pelengkap dalam struktur kimianya untuk mengkonfigurasi atom dengan cekap. Memandangkan protein lazimnya mempunyai beratus-ratus ikatan hidrogen "penderma" (biasanya oksigen) yang sepatutnya hampir dengan ikatan hidrogen "penerima" (biasanya nitrogen terikat kepada hidrogen), ia boleh menjadi sangat sukar untuk mencari konformasi di mana hampir setiap penderma hampir dengan penerima. Ketiga, terdapat contoh terhad untuk latihan kaedah eksperimen, jadi adalah perlu untuk memahami potensi interaksi tiga dimensi antara asid amino berdasarkan urutan 1D menggunakan maklumat tentang evolusi protein yang berkaitan.
Fizik pertama kali digunakan untuk memodelkan interaksi atom dalam mencari konformasi terbaik, dan kaedah telah dibangunkan untuk meramalkan struktur protein. Karplus, Levitt dan Warshel telah dianugerahkan Hadiah Nobel dalam Kimia 2013 untuk kerja mereka dalam simulasi pengiraan protein. Walau bagaimanapun, kaedah berasaskan fizik adalah mahal dari segi pengiraan dan memerlukan pemprosesan anggaran, jadi struktur tiga dimensi yang tepat tidak dapat diramalkan. Satu lagi pendekatan "berasaskan pengetahuan" ialah menggunakan pangkalan data struktur dan jujukan yang diketahui untuk melatih model melalui kecerdasan buatan dan pembelajaran mesin (AI-ML). Hassabis dan Jumper menggunakan elemen fizik dan AI-ML, tetapi inovasi dan lonjakan dalam prestasi pendekatan berpunca terutamanya daripada AI-ML. Kedua-dua penyelidik secara kreatif menggabungkan pangkalan data awam yang besar dengan sumber pengkomputeran gred industri untuk mencipta AlphaFold.
Bagaimanakah kita tahu mereka telah "menyelesaikan" teka-teki ramalan struktur? Pada tahun 1994, pertandingan Penilaian Kritikal Ramalan Struktur (CASP) telah ditubuhkan, yang bermesyuarat setiap dua tahun untuk menjejaki kemajuan ramalan struktur. Para penyelidik akan berkongsi urutan 1D protein yang strukturnya baru-baru ini diselesaikan, tetapi hasilnya belum diterbitkan. Peramal meramalkan struktur tiga dimensi menggunakan jujukan 1D ini, dan penilai secara bebas menilai kualiti keputusan yang diramalkan dengan membandingkannya dengan struktur tiga dimensi yang disediakan oleh ahli eksperimen (hanya disediakan kepada penilai). CASP menjalankan semakan buta sebenar dan merekodkan lonjakan prestasi berkala yang berkaitan dengan inovasi metodologi. Pada Persidangan CASP ke-14 pada tahun 2020, keputusan ramalan AlphaFold menunjukkan lonjakan prestasi sedemikian sehingga penganjur mengumumkan bahawa masalah ramalan struktur 3D telah diselesaikan: ketepatan kebanyakan ramalan adalah hampir dengan ukuran eksperimen.
Kepentingan yang lebih luas ialah kerja Hassabis dan Jumper secara meyakinkan menunjukkan cara AI-ML boleh mengubah sains. Penyelidikannya menunjukkan bahawa AI-ML boleh membina hipotesis saintifik yang kompleks daripada pelbagai sumber data, bahawa mekanisme perhatian (serupa dengan yang terdapat dalam ChatGPT) boleh menemui kebergantungan dan korelasi utama dalam sumber data, dan bahawa AI-ML boleh menilai sendiri kualiti hasil outputnya. AI-ML pada asasnya melakukan sains.
Masa siaran: Sep-23-2023